Zjawisko korozji metali, a szczególnie żelaza jest bardzo obszernym problemem i wiele jego aspektów nie zostało jeszcze do końca wyjaśnionych. Sama definicja tego zjawiska nastręcza badaczom wiele trudności. Dla większości z nich korozja oznacza wszystkie wzajemne oddziaływania metalu i jego otoczenia.
żelazo bardzo łatwo i szybko pod wpływem czynników zewnętrznych przechodzi ze stanu atomowego (metalicznego) w związki chemiczne. Każdy metal w zetknięciu z elektrolitem, a więc także w styczności z zewnętrznym środowiskiem korozyjnym wykazuje dążność do przechodzenia do roztworu w postaci jonowej. łatwość przechodzenia poszczególnych metali w stan jonowy wiąże się bezpośrednio z ich potencjałami normalnymi. Doświadczalne wyznaczenie potencjałów (mierzonych względem elektrody wodorowej i metalu zanurzonego w jego soli) pozwala na zestawienie metali w tak zwany szereg napięciowy.
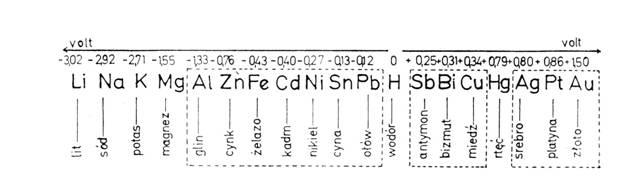
Rys. 1 Szereg napięciowy (przerywaną linią są zaznaczone metale występujące w obiektach zabytkowych w formie czystej bądź jako składniki stopów).
Przedstawiony szereg napięciowy metali pozwala przewidzieć ich odporność korozyjną. Szereg potencjałów normalnych wyraża kolejność, w której metale wykazują zdolność do wypierania się na wzajem z roztworów. Im dalej leżą od siebie metale tym pełniejsze będzie wypieranie metalu o wyższym potencjale przez metal o niższym potencjale. Tak więc przez łączenie dwóch różnych metali wytwarzamy pewnego rodzaju ogniwo, w którym (w elektrolicie) biegunem dodatnim będzie zawsze metal znajdujący się bliżej końca szeregu napięciowego, biegunem dodatnim – będący bliżej początku. Należy pamiętać w tym miejscu, że niewłaściwe połączenie metali mogą doprowadzić do dodatkowych, niszczących procesów korozyjnych.
Z konserwatorskiego punktu widzenia jako korozję należy rozumieć zespół procesów chemicznych powodujących zmianę powierzchni oraz struktury substancji zabytkowej. Rezultatem tych procesów są zmiany barwy, struktury, tekstury, własności wytrzymałościowych i technologicznych oraz deformacje. Długotrwałe działanie korozji prowadzi do całkowitego zniszczenia obiektu!
Możemy wyróżnić kilka procesów korozyjnych, wywołujących charakterystyczne zniszczenia żelaza :
· Korozja wżerowa
· Międzykrystaliczna
· Warstwowa
· Kanalikowa
· Atmosferyczna
· Ziemna
· Wodna
· Bakteryjna
· Kruchość wodorowa
· Psywacyjno-aktywacyjna
· Naprężeniowa
· Gazowa
· Korozja w elektrolitach
W zależności od rodzaju zniszczeń możemy wyróżnić :
· Korozję równomierną – jest najmniej szkodliwą z wymienionych poniżej
· Plamistą – występuje w różnych miejscach powierzchni, w postaci plam o niewielkiej głębokości wżeru. Ten rodzaj zniszczeń jest podobny do korozji równomiernej
· Wżerową – występują duże zagłębienia w jednym miejscu na powierzchni metalu
· Podpowierzchniową – powstaje i rozprzestrzenia się pod powierzchnią metalu, gdzie gromadzą się produkty korozji, co prowadzi do rozwarstwiania się metalu.
· Międzykrystaliczną – rozprzestrzenia się w głąb żelaza po przez ziarna kryształu
· Szczelinową – uwidacznia się w miejscach nieszczelnych połączeń żelaza, np. gwinty, nity

W większości żelazne obiekty ulegają zniszczeniu w wyniku przebywania w środowiskach: atmosferycznym, ziemnym i wodnym. Z racji tego, iż większość poszukiwaczy „skarbów” ma do czynienia z obiektami wyciągniętymi z ziemi, niniejszym opracowaniu skupiono się na środowisku ziemnym z pominięciem środowiska wodnego i atmosferycznego.
Procesy korozyjne, którym ulegają obiekty z żelaza w złożonym środowisku zimnym, uzależnione są od: wilgotności gleby, kwasowości, napowietrzenia, temperatury, drobnoustrojów oraz od tekstury gleby. Różnice w nawilgoceniu gleby uzależnione są od opadów atmosferycznych oraz stopnia zdolności zatrzymania przez nią wilgoci. W miarę wzrostu wilgotności gleby jej korozyjna aktywność wzrasta aż do momentu osiągnięcia pozornych wartości optymalnych (krytycznych), przy których aktywność ta maleje. Spowodowane jest to tym, iż przy dużych wilgotnościach zmniejsz się dostęp tlenu do obiektu, który jest niezbędnych czynnikiem depolaryzacji katodowej żelaza (proces korozji).
Gleby wykazują pH w granicach od 6 do 7,5, a więc mają odczyn zbliżony do obojętnego. Jednak spotyka się także gleby o odczynie alkalicznym (7,5 – 9 pH) należą do nich głównie gleby gliniaste, oraz gleby kwaśne (3 – 6 pH) do nich należą gleby bagniste i humusowe. Wraz ze zmniejszeniem pH gleby wzrasta jej aktywność korozyjna, co przejawia się dużymi zniszczeniami obiektów. Odczyn alkaliczny wiąże się z ilością występujących w glebie rozpuszczonych w wodzie soli. Szczególnie szkodliwe są sole chlorkowe, aktywizujące procesy korozyjne żelaza. W glebie spotyka się najczęściej kationy wapnia, potasu, sodu i magnezu. Mogą one tworzyć w ziemi nierozpuszczalne tlenki i węglany, których osady bardzo często spełniają rolę warstewek ochronnych na powierzchni metalu, zmniejszając aktywność korozji. Jednak znajdujące się w glebie sole mogą prowadzić do wzrostu aktywności biologicznej mikroorganizmów, wpływając tym na przyśpieszenie korozji.
Stopień napowietrzenia gleby jest jednym z najważniejszych czynników przyczyniających się do zwiększenia szybkości korodowania obiektu. Badania udowodniły, iż wraz ze wzrostem głębokości maleje szybkość korozji.
W źle napowietrzanych glebach, zawierających duże ilości siarczanów może nastąpić wzrost biologicznej aktywności korozyjnej bakterii anaerobowych. Tlen zawarty w anionie siarczanu uwalniany jest w wyniku działalności bakterii redukujących siarczany. Powstały w ten sposób tlen przyśpiesza proces korozyjny. Obok uwalniania tlenu, następuje zakwaszanie gleby w skutek tworzenia się siarkowodoru. Co z oczywistych względów dodatkowo przyczynia się do przyśpieszenia procesów korozji.
Problem usuwania nawarstwień korozyjnych z powierzchni żelaza jest równie obszerny i skomplikowany jak zagadnienia zachodzących na niej procesów korozyjnych. W przypadku żelaznych obiektów zabytkowych najczęściej mamy do czynienia z przedmiotami o skomplikowanych kształtach, połączeniach, nitowaniach, zachodzących na siebie płaszczyzn metalu, pokrytych bardzo grubymi nawarstwieniami produktów, których usunięcie nastręcza wiele trudności. Obiekty te często są zdobione lub też mają połączenia z materiałami organicznymi, co w znacznym stopniu ogranicza stosowanie danej metody oczyszczającej.
Konserwację metalu można podzielić ogólnie na dwa procesy. Pierwszy to proces oczyszczania powierzchni metalu, drugi to zabezpieczanie przedmiotu przed dalszym niszczeniem. Oba procesy są równie ważne i jeśli mówimy o konserwacji przedmiotu to nie można się skupić tylko na oczyszczeniu przedmiotu i pominąć proces zabezpieczenie przed dalszym niszczeniem.
Oczyszczanie powierzchni metalu.
Proces oczyszczania skorodowanych powierzchni można podzielić na 5 metod :
1 – mechaniczne
2 – chemiczne
3 – redukcyjne
4 – termiczne
5 – fizyczne
Metody mechaniczne.
Mechaniczne oczyszczanie nawarstwień korozyjnych jest najstarszą ze stosowanych metod usuwania produktów korozji. Ręczne oczyszczanie mechaniczne przeprowadza się najczęściej przy użyciu takich narzędzi jak: igły, skrobaki, przecinaki, szczotki itp., które umożliwiają rozkruszenie i odrywanie produktów korozji. Stosuje się również szlifierki, wiertarki dentystyczne, pozwalające na usuwanie korozji z miejsc trudno dostępnych wżerów. Oczyszczanie mechaniczne umożliwia zastosowanie innej metody (chemicznej lub redukcyjnej), dzięki której osiąga się znaczne rozluźnienie lub spulchnienie produktów korozji.
Wśród tych metod można wyróżnić :
a. Piaskowanie – polega na rzucaniu pod ciśnieniem na skorodowaną powierzchnię odpowiedniego materiału ściernego, np. piasku rzecznego, drobnego szkła, korundu lub śrutu żeliwnego.,
Piaskowanie jest dość dobrą metodą usuwanie nawarstwień z powierzchni żelaza, ale jak w każdym przypadku metoda ta jest uzależniona od rodzaju przedmiotu i stopnia jego zniszczenia. Należy także dobrać odpowiednie ścierniwo i ciśnienie robocze. Piaskowanie niestety nie usuwa z powierzchni przedmiotu soli agresywnych, które inicjują procesy korozji. Nie usuwa także produktów korozji z porów i wżerów.
Metody termiczne.
Oczyszczanie termiczne polega na poddawaniu skorodowanej powierzchni działaniu wysokich temperatur. Zabieg ten najczęściej przeprowadza się przy użyciu palnika gazowego lub acetylenowo-tlenowego. Rdzę nagrzewa się silnie, ale w taki sposób, aby nie podwyższać znacznie temperatury żelaza (rdzenia obiektu). W skutek gwałtownego przechodzenia w parę wilgoci zawartej w produktach korozji oraz różnej rozszerzalności termicznej, następuje spękanie i odrywanie się rdzy od podłoża. W tym procesie następuje także przeistoczenie się częściowe rdzy w czarne tlenki żelaza. Jest to dobry i szybki sposób na oczyszczanie dużych powierzchni żelaznych, i przygotowanie ich pod pokrycie powłoką ochronna. Jednak nie jest to dokładna metoda i nie pozwala na precyzyjne oczyszczenie bardziej skomplikowanych przedmiotów, a zbyt długie wygrzewanie może prowadzić do odwęglania obiektu, co w znaczny sposób przyczyni się do kruchości obiektu. Procesu odrywania nie da się kontrolować, i czasami się zdarza, że rdza odrywa się z kawałkami powierzchni metalu, niszcząc ją w ten sposób. Ogólnie można stwierdzić, iż tą metodę należy stosować do obiektów o zdrowym rdzeniu! Metoda ta nie nadaje się do zdobionych inkrustacjami przedmiotów!! Nie należy jej także stosować do obiektów nie oczyszczonych wstępnie z piasku i gliny (np. obiektów archeologicznych), gdyż wysoka temperatura powoduje twardnienie wszelkich nalotów z gliny i krzemionki i jednoczesne zespolenie ich z rdzą, przez co stają się praktycznie nie rozpuszczalne dla wielu środków chemicznych.
Metody redukcyjne.
3. Redukcyjne metody usuwania produktów korozji oparte są na wykorzystaniu zjawiska redukcji elektrochemicznej lub redukcji elektrolitycznej. Oprócz wyżej wymienionych metod istnieje jeszcze redukcja za pomocą gazowego wodoru. We wszystkich wymienionych tu metodach redukcji czynnikiem ułatwiającym oczyszczenie jest gazowy wodór, wydzielający się podczas zachodzących redukcji. Działanie wodoru polega na mechanicznym spulchnianiu i rozluźnianiu produktów korozji.
a. Redukcja elektrochemiczna (autoliza)
W redukcji elektrochemicznej oczyszczany obiekt żelazny traktowany jest najczęściej jako katoda. Wydziela się na niej gazowy wodór w wyniku redukcji metalicznego cynku, ołowiu, glinu (aluminium), w wyniku działania elektrolitu. Oczyszczanie obiektu można też prowadzić traktując obiekt jako anodę, wówczas na skorodowanej powierzchni wydzielać się będzie tlen, powodując rozluźnianie produktów korozji. Proces oczyszczania można przyśpieszyć przez zwiększenie kontaktu redukowanego metalu z oczyszczanym obiektem, po przez podniesienie temperatury oraz zwiększenie stężenia elektrolitu. Jako elektrolity stosuje się roztwory wodorotlenku sodu, kwasów organicznych, oraz soli tych kwasów.
Oto 3 sposoby zastosowania autolizy:
- wg Kreftinga
Przedmiot, oczyszczony do czystego metalu, owinięto taśmą cynkową o grubości 0,2-0,3 mm i o szerokości 0,5-1 cm, w ten sposób, żeby cynk ściśle przylegał do oczyszczonego miejscami metalu. Tak przygotowany obiekt przeniesiono do 3% roztworu ługu sodowego, wolnego od chloru. Na średni skorodowanym obiekcie zabieg ten trwał 24 godziny. Po zakończeniu redukcji obiekt wyjęto z kąpieli i mechanicznie usunięto rozluźnione warstwy rdzy.
- wg Rhousopoulosa
Taśmę cynkową nakłada się bezpośrednio ma skorodowaną powierzchnię, bez wykonywania miejsc styku z czystym metalem, pomiędzy taśmę a rdzę upycha się sproszkowany cynk. Redukcje na tak przystosowanym obiekcie prowadzi się w 10% roztworze ługu i powtarza się ją dwukrotnie.
- wg Plenderleitha
Przy obiektach bardziej skorodowanych zaleca stosowanie wodorotlenku sodu z cynkiem granulowanym, a jednocześnie w podwyższonej temperaturze.
Do redukcji elektrochemicznej można stosować jak elektrolity także: wodorotlenek potasu, cjanek potasu, kwas octowy, kwaśny węglan amonu, wodorotlenek sodu o stężeniu dochodzącym nawet do 20% (jednak przy mniejszych obiektach i bardziej wartościowych zaleca się stosowanie roztworu 10%, gdyż wolniejszy przebieg procesu oczyszczania pozwala na lepszą jego kontrolę), winian sodu-potasu. Należy pamiętać, iż użycie cynku i wodorotlenku sodu w procesie oczyszczania jest reakcją burzliwą i egzotermiczną (wydziela ciepło) i zaleca się dużą ostrożność!!!
Innym sposobem zastosowania autolizy w procesie oczyszczania jest zastosowanie pas odrdzewiających (oczyszczających). Sporządza się je z pyłu cynkowego i kwasu siarkowego. Pasty pozwalają na miejscowe oczyszczenie skorodowanej powierzchni.
b. Redukcja elektrolityczna
W redukcji elektrolitycznej wykorzystuje się zjawisko przepływu prądu elektrycznego przez elektrolit, który przyśpiesza proces oczyszczania. Podobnie jak i przy redukcji elektrochemicznej, czynnikiem spulchniającym i rozluźniającym rdzę jest gazowy wodór lub tlen, w zależności od sposobu prowadzenia elektrolizy. Podczas procesu anodowego oczyszczany przedmiot taktowany jest jak anoda, katodą jest natomiast płyta (płyty) cynkowe, miedziane lub żelazne. Wydzielający się na obiekcie tlen gazowy działa mechanicznie na warstwy tlenków, spulchniając je i rozluźniając, ale też w dużym stopniu rozpuszczając również metal, i powodując dość duże ubytki metalu. Z tego to powodu, po mimo znacznie szybszego procesu oczyszczania, nie należy stosować anodowej redukcji elektrolitycznej.
Znacznie lepsze efekty osiąga się po przez zastosowanie katodowego traktowania oczyszczanego żelaza. Czynnikiem spulchniającym i rozluźniającym korozję jest burzliwie wydzielający się wodór na powierzchni oczyszczanego przedmiotu. Przy oczyszczaniu stosuje się prąd stały , o napięciu około 12 V. Jednak najważniejszym czynnikiem w tym procesie jest natężenie prądu, uzależnione od rodzaju elektrolitu i wielkości elektrod. Dlatego też przy elektrolizie operuje się pojęciem gęstości prądu. Przyjmuje się, że gęstość stosowanego prądu powinna wynosić około 10 amperów na decymetr kwadratowy katody, co zapewnia stałe i silne wydzielanie się wodoru.
Występujące na początku zabiegu nawarstwienia na powierzchni metalu (katody) powodują, że opór wewnętrzny układu jest dość wysoki, należy wówczas stosować wyższe natężenie prądu. Po pewnym czasie opór wewnętrzny maleje (w wyniku częściowego usunięcia nawarstwień), wzrasta więc natężenie prądu. Aby utrzymać stała gęstość prądu, należy w tym momencie zwiększyć opór zewnętrzny układu. Najlepsze rezultaty uzyskuje się przy zastosowaniu dwóch anod, zawieszonych w równej odległości od katody (obiektu).
Do przeprowadzenia elektrolizy stosuje się elektrody anodowe wykonane ze różnych metali. Jednak należy pamiętać, że nie wszystkie są odpowiednie. Anody żelazne niszczeją podczas elektrolizy , odrywają się od nich dość duże kawałki z tlenków metalu, ponadto na anodach osadzają się produkty połączeń chlorkowych, jeżeli obiekt zawierał jony chlorkowe (sole). Elektrody grafitowe lub węglowe powodują powstawanie w środowisku alkalicznym trwałe, trudno usuwalne osady na oczyszczanym obiekcie. Najodpowiedniejsze są anody ołowiane lub ze stopu ołowiu z antymonem. Jako elektrolitu można używać roztworów kwasów, zasad lub soli. Elektroliza w środowisku alkaliczny przebiega znacznie wolniej, ale jest wówczas bardziej bezpieczna i dokładniejsza.
Miejsce styku przewodu miedzianego (doprowadzającego prąd) z obiektem musi być mechanicznie oczyszczone do rdzenia metalicznego. Grubość przewodu uzależniona jest od wielkości przedmiotu. średni czas oczyszczania średnio skorodowanego przedmiotu wynosi 48 godzin. Po upływie tego czasu, obiekt opłukuje się w kąpielach wodnych, a spulchnione nawarstwienia usuwa się przez pocieranie szczotką. Jeżeli obiekt nie został oczyszczony, zabieg można powtórzyć.
Przy wyjmowaniu obiektów między kolejnymi kąpielami należy zmieniać bieguny źródła prądu, pozostawienie obiektów w stanie wyjściowym powoduje osadzanie się na katodzie (obiekt) zanieczyszczeń pochodzących z elektrolitu bądź z anody.
c. Redukcja gazowym wodorem
Stosowanie redukcji gazowym wodorem jest bardzo niebezpieczną metodą zarówno dla osoby przeprowadzającej ten zabieg, jak i dla samego oczyszczanego przedmiotu. Metoda ta nazywana jest metodą Hertwicha. Polega na wytworzeniu gazowego wodoru w aparacie Kippa, który jest następnie przepuszczany przez ogrzewaną rurkę (palnikiem), w którym znajduje się oczyszczany przedmiot. Metoda ta praktycznie nie jest stosowana w konserwatorstwie.
Metody redukcji elektrochemicznej i elektrolitycznej uznawane są za jedne z najskuteczniejszych metod oczyszczania skorodowanych przedmiotów. Jednak zakres ich wykorzystania w dużym stopniu uzależniony jest od wielkości przedmiotu. Trwałe połączenia z innymi metalami także w dużym stopniu utrudniają ich stosowanie.
Przy użyciu metod redukcyjnych mogą jednak występować zjawiska niekorzystne. Na skutek zachodzącego wydzielania się wodoru następuje nawodornienie powierzchni oraz głębszych partii żelaza. Prowadzi to do korozji wodorowej, wywołującej kruchość wodorową metalu, przy której obserwuje się znaczne obniżenie własności wytrzymałościowych metalu., bez widocznych zmian na powierzchni. Proces ten dotyczy w dużej mierze przedmiotów o zwiększonych własnościach wytrzymałościowych, przedmiotów które były wcześniej specjalnie nawęglane alby zwiększyć ich wytrzymałość mechaniczną (np. miecze). Przy tego typu przedmiotach należy przeprowadzić badania czy taki rodzaj oczyszczania nie spowoduje zbyt dużego zniszczenia i osłabienia przedmiotu.
Metody fizyczne.
W fizycznej metodzie usuwania nawarstwień z powierzchni metalu stosowane są ultradźwięki, wywołujące w cieczach intensywne mechaniczne ruchy mieszające i wstrząsające, umożliwiające usuwanie zanieczyszczeń z powierzchni obiektu. Z wielu badań przeprowadzonych nad wykorzystaniem ultradźwięków do oczyszczania wynika, że w zabiegach tych można stosować zarówno ultradźwięki o małej częstotliwości – 25 kHz, jak i o wielkiej, rzędu 300 – 1000 kHz. Działanie praktyczne tych częstotliwości jest różne, ultradźwięki o małych częstotliwościach nadają się do usuwania nawarstwień twardych. Natomiast o częstotliwościach dużych mogą być stosowane do usuwania cząsteczek brudu, warstewek tłuszczu i lakierów. Przy doborze częstotliwości ważna jest wielkość przedmiotu. W przypadku przedmiotów większych lepsza jest niższa częstotliwość ultradźwięków, ponieważ wypromieniowana wiązka nie jest równoległa i dlatego dzięki załamaniu lub ugięciu dźwięku łatwiej dochodzą do wszystkich oczyszczanych miejsc.
Obok mechanicznego działania ultradźwięków, do usuwania nawarstwień konieczne jest stosowanie środków chemicznych, które wspomagają działanie mechaniczne. Jako substancje wspomagające można stosować kwasy, zasady lub ich sole. Czynnikiem przyśpieszającym oczyszczanie jest też wyższa temperatura. Ultradźwięki pozwalają na bardzo dobre oczyszczenie z produktów korozji lub też wyciągnięcie użytych substancji chemicznych ze szczelin i wżerów.
Metody chemiczne.
Czyszczenie metali środkami chemicznymi, przede wszystkim kwasami, w celu uzyskania powierzchni wolnej od produktów korozji oraz innych zanieczyszczeń, jest jednym z najstarszych zabiegów oczyszczani powierzchni metalu. Podobnie jak i pozostałe metody tak i ta ma swoje wady: narażenie metalu na możliwość rozpuszczania się oraz trudności w usunięciu resztek stosowanych środków chemicznych z powierzchni oczyszczonego metalu, które powodować mogą korozję wtórną. Jednak w pewnych przypadkach, ze względu na rodzaj i charakter zabytku, jego stan zachowania, wielkość czy rodzaj połączeń z innymi metalami, nie można odstąpić od działania chemicznego. Dość często zdarza się, że stan obiektu jest bardzo zły i trzeba usunąć z niego zanieczyszczenia wtórne w postaci farb czy lakierów. Metody chemiczne są tez bardziej dostępne i ekonomiczne, nie wymagają specjalistycznych urządzeń i są stosunkowo proste do wykonania. Co jest bardzo dużym atutem na rzecz tych metod.
Najczęściej do rozpuszczania rdzy stosowane są roztwory rozmaitych kwasów o różnych stężeniach. Ich działanie sprowadza się głównie do rozpuszczania i usuwania produktów korozji, rozpuszczania metalicznego żelaza oraz do spulchniania i rozluźniania produktów korozji. Rozpuszczanie żelaza w skorodowanym obiekcie przez działanie kwasu następuje w wyniku reakcji katodowej, oczyszczane żelazo stanowi katodę a rozpuszczane produkty korozji są biegunami ujemnymi.
Najważniejszym czynnikiem na który musimy zawsze zwracać uwagę podczas stosowania tej jak i innych metod jest stopień zachowania przedmiotu. Od tego zależy rodzaj kwasu i jego stężenie. Przy przedmiotach pokrytych grubymi nawarstwieniami i zdrowym rdzeniu możemy zastosować kwasy o dużych stężeniach, jednak zalecane jest zawsze mniejsze stężenie, gdyż obiekt jest w mniejszym stopniu narażony na trawienie.
Stosuje się kąpiele odrdzewiające zawierające kwasy nieorganiczne i organiczne, takie jak: siarkowy, solny oraz ortofosforowy, który jest najczęściej stosowanym środkiem do usuwania rdzy, kwas szczawiowy, cytrynowy, winowy. Używa się także innych związków jak: kwaśny węglan sodu, kwaśny węglan amonu oraz chlorek amonu.
Bardzo istotnym elementem w konserwacji obiektów metalowych jest zabezpieczenie go przed dalszym niszczeniem. Proces ten jest dwu etapowy. Pierwszym etapem jest zastosowania inhibitora korozji, który stabilizuje procesy korozyjne, po przez stworzenie na powierzchni metalu cieniutkiej warstewki nierozpuszczalnych związków żelaza. Najlepszym i najbardziej popularnym na rynku środkiem do pasywacji żelaza jest Tanina. Tanina nie tylko pasywuje produkty korozji, ale także wiąże je z podłożem metalicznym przez co w znacznym stopniu przyczynia się do wzmocnienia skorodowanego obiektu. Wiązania tanatów bazują na wiązaniach żelowych. Dlatego nie wolno podgrzewać obiektów pokrytych tanina, gdyż zetnie się tanina i straci swoje właściwości wzmacniające i stabilizujące. Drugim etapem jest odcięcie powierzchni metalu od warunków atmosferycznych. Najskuteczniejszą ochronę moim zdaniem daje pokrycie cieniutką warstewką 10 % Paraloidu B 44 w Ksylenie. A następnie nałożenie na nią warstwy wosku w postaci pasty Cosmoloid 80H w benzynie lakowej. Paraloid B44 daje trwała i odporną na działania niekorzystnych warunków środowiskowych. Warstwa ta jest dość elastyczna więc nie pęka w wyniku starzenia się. Wosk uzupełnia wszelkie niedociągnięcia i daje hydrofobową warstwę dla wody. Wosk nie powoduje osadzania się na obiekcie kurzu i innych brudów.
Kilka uwag o domowych metodach.
Większość z nas zastanawia się ja oczyścić swój przedmiot i jakiej użyć metody. Niestety bardzo często aby oczyścić nasze skarby zmuszeni jesteśmy do przetworzenia specjalistycznych konserwatorskich metod na domowe warunki. Zazwyczaj pozbawieni jesteśmy większości odczynników i środków chemicznych a także specjalistycznego sprzętu. Dlatego też poszukuje się innych środków opartych na zasadach konserwatorski, które umożliwią oczyszczenia naszych obiektów. Ogólnie mówiąc domowe metody są bardzo zbliżone do tych specjalistycznych, ale zazwyczaj oparte są na tańszych środkach i mniej specjalistycznych urządzeniach. Należy jednak pamiętać, że nie istotne jest jakim sposobem oczyścimy przedmiot, ale istotne jest to czy nasz przedmiot nie straci swojej wartości i czy uda nam się go zachować dla kolejnych pokoleń. Nie sztuką jest tylko oczyścić przedmiot, który niezabezpieczony przed dalszym niszczeniem po kilku latach rozpadnie się albo straci swoją wartość. Jeśli tylko możemy powinniśmy stosować jak najbardziej bezpieczne środki aby, sam proces oczyszczenie nie spowodował z czasem dalszego niszczenia obiektu.
Najbardziej rozpowszechnionym domowym sposobem jest użycie elektrolizy. Z racji, niewielkich kosztów zakupienia prostownika i niewielkich kosztów na elektrolit jest to najbardziej skuteczna metoda oczyszczania i najbardziej rozpowszechniona. Stosując prostowniki o napięciu 12 V i o natężeniu ok. 7 A uzyskuje się bardzo dobre wyniki. Niestety elektroliza powoduje delikatne zżeranie metalu, czego efektem są nieraz dużo większe wżery niż przed oczyszczeniem. Dlatego należy kontrolować proces oczyszczania! Często zdarza się, że nie cała powierzchnia zostanie oczyszczona. Należy się wtedy zastanowić czy nie zmienić metody na inną i czy nie zastosować np. pasy zamiast dalej trawić obiekt, czego efektem będzie nierównomiernie nadżarta powierzchnia.
Jako elektrolity w domowych warunkach używa się praktycznie tylko dwóch roztworów. Roztworu soli kuchennej i roztworu NaOH (a raczej roztworu z Kreta). Każdy z tych środków ma swoje wady i zalety. Sól kuchenna jest najtańszym elektrolitem i mało szkodliwym dla ludzi. Niestety nie można powiedzieć tego samego o obiekcie. Sól jest największym wrogiem każdego metalu, korozja z udziałem jonów chlorkowych jest praktycznie najgroźniejszą i czyniącą największe szkody przedmiotom wykonanym z metalu i nie tylko. Jeśli jednak już stosujemy sól kuchenna jako elektrolit pamiętajmy o możliwie jak najdłuższym płukaniu obiektu pod bieżącą wodą lub o ile to możliwe wodą destylowaną. W ten sposób wypłuczemy znaczną ilość soli, która wniknęła w metal. O destruktywnym wpływie soli możemy się przekonać dość szybko jeśli tylko warunki przechowywania zmienią się na bardziej niekorzystne ( np. z większą wilgotnością). Roztwór NaOH jest pod tym względem bardziej bezpieczny dla obiektu i stosowanie jego daje lepsze efekty w procesie oczyszczania. Niestety jest droższy i żrący.
Dość często ostatnimi czasy zaczyna się stosować autolizę. Jest to też dość skuteczna i szybka metoda. Jako elektrolitu używa się najczęściej NaOH (czyli w naszym przypadku Kreta). Można używać także kwasów ale ich reaktywność jest mniejsza i proces oczyszczania zachodzi wolniej. Do autolizy stosuje się najczęściej taśmę aluminiową lub też popularną folię aluminiową do pieczenia (niestety szybko się rozpuszcza, gdyż jest za cienka). Autoliza jest dobrym sposobem na oczyszczanie mniejszych przedmiotów, gdyż mamy większą kontrolę nad procesem oczyszczania i jest to proces bardziej dokładny.
Bardzo dobrą metodą choć mniej popularna jest piaskowanie. Większość z nas, nie posiada niestety piaskarek, jednak warto jest zainwestować w tego rodzaju urządzenie. Wystarczy dokupić specjalny pistolet do piaskowania i podłączyć do kompresora i zbiornika na kruszywo. Koszt kompresora waha się od 600 zł wzwyż, cena zależna jest od rodzaju kompresora. Piaskowanie daje znakomite efekty przy powierzchniowym oczyszczaniu przedmiotu z produktów korozji. Należy pamiętać, że nie ma idealnej metody na oczyszczenia każdego przedmiotu i o ile do jednego obiektu piaskowanie mogłoby być dobrą metodą to wcale nie znaczy, iż będzie nadawać się do innych obiektów. Piaskowanie daje dobre efekty przy oczyszczaniu wszelkiego rodzaju hełmów, broni, bagnetów i wielu innych przedmiotów. Nie powoduje pogłębiania się wżerów w obiektach i powierzchnia przedmiotu nie wygląda jak „powierzchnia księżyca”, pełna kraterów, po użyciu elektrolizy. Nie zawsze jednak w pełni można usunąć wszystkie nawarstwienia, dlatego trzeba użyć dodatkowo innej metody. Piaskowanie nie wyciąga produktów korozji z porów i wżerów, co powoduje że niezpasywowane stanowią ogniska dalszej korozji, ale po zabezpieczeniu obiekt wygląda dużo lepiej niż po elektrolizie. Należy pamiętać, że każdy ma swoje ulubione metody i każda ma swoich zwolenników i przeciwników, ale najważniejsze jest to aby wybrać najlepszą metodę do oczyszczenia danego obiektu, co czasami wiąże się z zastosowaniem kilku metod do oczyszczenia jednego przedmiotu.
Drugą równie ważna rzeczą jest zabezpieczenie przedmiotu przed dalszą korozją. Niestety w tym wypadku domowe sposoby są najbardziej narażone na niepowodzenie lub też na krótkotrwałe działanie. Najpopularniejszymi metodami są malowanie farbami antykorozyjnymi, pokrywanie powierzchni lakierami, smarami, olejami lub też pozostawianie obiektu bez jakiegokolwiek zabezpieczenia. Niestety każdy z tym sposobów jest bardzo niewystarczający.
Pokrywanie wszelkiego rodzaju farbami o ile obiekt nie był pierwotnie pokryty farbą jest posunięciem bardzo nieestetycznym. Bardzo często spotyka się pomalowane na czarno hełmy, broń czy bagnety, które wyglądają dość paskudnie. Jedyne czym można się pocieszyć w tym momencie jest to, że przedmiot chociaż w pewnym stopniu jest zabezpieczony przed korozją. Smarowanie olejami i samarami jest o tyle skuteczne i ile w miarę często naciera się dany przedmiot. Stanowią one hydrofobową barierę dla wody, a znaczna ich gęstość ogranicza dostęp tlenu do powierzchni metalu. Niestety oleje są niewdzięczne dla konserwacji ponieważ, szybko ściekają i z czasem się utleniają, przez co powłoka z czasem staje się coraz cieńsza i bardziej przepuszczalna. Czasami zdarza się, że użyte oleje czy smary wnikają w metal i go przebarwiają przez co obiekty tracą swą estetykę. Smary i oleje mają jeszcze jedna nieszczęsną wadę, gdyż łapią tony kurzu i brudu, przez co obiekt wygląda niezbyt estetycznie. Chyba najlepszym sposobem dostępnym w domu i sklepie, jest pokrywanie cienką warstwa lakieru. Niestety tak jak poprzednie sposoby tak i ten ma szereg wad. Najbardziej denerwującą i krytykowaną przez większość osób wadą jest połyskliwość powłoki lakierowej. Aby chociaż w pewnym stopniu zmniejszyć połyskliwość można nieco rozcieńczyć lakier, nie za bardzo aby nie stracił swych ochronnych właściwości. Lakier odcinając dostęp tlenu i wilgoci chroni obiekt przed dalszą korozją. Jednak używanie zwykłych lakierów wiąże się z tym że nie są to produkty przeznaczone do metalu. Z czasem ich powłoki utleniają się i starzeją, co prowadzi do pękania i złuszczania się ich z powierzchni metalu, co w dalszej kolejności powoduje odsłonięcie i narażenie na korozję. Istnieje wiele innych domowych sposobów na zabezpieczanie ich przed niszczeniem, ale żaden tak naprawdę nie zabezpiecza ich w większym stopniu, przed dalszą korozją. Wiele osób może powiedzieć, iż mają zakonserwowane obiekty w przedstawiony powyżej sposób lub jakiś inny i że nic im się nie dzieje. Jednak przy takim sposobie zabezpieczania i przy większej zmianie wilgotności w dość szybkim czasie w mniejszym lub większym stopniu zaczęły by korodować.
Bardzo popularne są także metody chemiczne. Paleta dostępnych środków jest bardzo duża a pomysłowość ludzi jeszcze większa, dlatego też nie sposób wymienić wszystkich stosowanych środków. Stosuje się wszystko od słabych kwasów cytrynowego czy octowego po mocne kwasy azotowy czy siarkowy (czytałem o przypadkach stosowania kwasu ogórkowego i mlekowego co potwierdza fakt, że wyobraźnia ludzka nie zna granic). Stosuje się także wszelkiego rodzaju dostępne zasady, najczęściej używa się jednak NaOH zawartego w popularnym Krecie. Popularne są także wszelkiego rodzaju kąpiele w ropie, nafcie, benzynie czy preparatach penetrujących jak np. WD-40. Należy jednak pamiętać, że większość z tych środków tak naprawdę nie powinna być stosowana do oczyszczania metalu. Bardzo często środki te zawierają bardzo dużo szkodliwych substancji, które bardzo niekorzystnie wpływają na metal i mogą powodować wtórna korozję. Należy starać się używać jak najbardziej czystych odczynników chemicznych, gdyż przyczyni się to do większej żywotności naszych obiektów.
Nie ma dobrych domowych sposobów na pasywację produktów korozji przed dalszym niszczeniem obiektów. Tylko stosowanie inhibitorów korozji pozwoli na wstępne zabezpieczenie i „dezaktywowanie” korozji. Najlepszym i najbardziej popularnym na rynku środkiem do pasywacji żelaza jest Tanina. Tanina nie tylko pasywuje produkty korozji, ale także wiąże je z podłożem metalicznym przez co w znacznym stopniu przyczynia się do wzmocnienia skorodowanego obiektu. Tanina nie wiąże jak większość impregnatów, jej wiązania polegają na wiązaniach żelowych. Dlatego nie wolno podgrzewać obiektów pokrytych tanina, gdyż zetnie się tanina i straci swoje właściwości wzmacniające i pasywujące.
Najistotniejsze jest dla nas to aby uzmysłowić sobie i wybrać jak najlepszą metodę dla zabezpieczenia obiektu. Czasami pomalowanie farbą będzie w stu procentach satysfakcjonującą metodą np. w przypadku malowania hełmów czy elementów pojazdów itp. Tak jak smarowanie elementów broni czy głowic bagnetów będzie także dobrym posunięciem to nie znaczy że będzie dobrze wyglądało na innych przedmiotach.
Przykłady konserwacji przedmiotów żelaznych.
Przedmiotem konserwacji jest płyta kominkowa z XVII/XVIII w..
Płytę żeliwną o wymiarach 1,20 m x 0,90 m pokrywała gruba i zwarta warstwa produktów korozji. Miejscami widoczne były rdzawe naloty, złuszczenia warstw korozyjnych i zabrudzenia warstwą cementu, co wyraźnie zmniejszało wartość estetyczną obiektu. Z racji wielkości obiektu i bardzo zwartych nawarstwień najbardziej odpowiednią metodą ich usunięcia było piaskowanie. Metody chemiczne okazały się niezbyt skuteczne z racji ich powolnego i niedokładnego działania (miejsca zagłębione oczyszczały się bardzo źle). Jako ścierniwo zastosowano piasek szklarski. Oczyszczanie trwało łącznie ok. 14 godzin. Po oczyszczeniu z nawarstwień korozyjnych całą płytę przecierano watą stalową, aby zmniejszyć powstałe zmatowienie powierzchni płyty (ścierniwo powoduje powstanie na powierzchni przedmiotu szeregu mikrorys, co powoduje zmatowienie obiektu). Przy tak dużym obiekcie przecieranie watą trwało ok. 2 godzin. Na tak przygotowaną powierzchnię nałożono warstwę Taniny. Co spowodowało znaczne ściemnienie obiektu. Nadmiar tanatów (produkty reakcji wiązania taniny z metalem) usunięto z powierzchni przy użyciu waty stalowej, dzięki czemu powierzchnia nabrała bardziej połyskliwego charakteru i delikatnego połysku metalicznego. Ostatnim etapem było zabezpieczenie powierzchni płyty po przez nałożenie cienkiej warstwy lakierowej Praloidu B 44. Etapem wieńczącym proces zabezpieczania przed powtórną korozją było nałożenie wosku mikrokrystalicznego (Cosmoloid) i wypolerowanie powierzchni przy użyciu gazy lub szmatki.
Płyta przed konserwacją:

(fot. A. Tomaszewska)
Płyta po konserwacji:

(fot. A. Tomaszewska)
Element kopii zbroi wykonanej w XIX w. (Nakarczek)..
Do oczyszczenia tego przedmiotu zastosowano także piaskowanie z użyciem piasku szklarskiego. Przedmiot pokryty był łuszczejącą warstwą farby (poprzednia konserwacja z lat 60 ). Miejscami pod warstwą farby tworzyły się ogniska korozji, widoczne jako rdzawe miejsca z odpadającą warstwą farby. Obiekt dodatkowo był powyginany miejscami (chyba z nieudolnej próby dopasowania do pozostałych elementów zbroi). W pierwszej kolejności należało wyprostować pogięte miejsca. Najlepszy efekty przynosiło wyklepywanie drewnianym lub gumowym motkiem, gdyż nie pozostawiały śladów po uderzeniach na powierzchni metalu. Następnie oczyszczono powierzchnię z korozji i resztek farby po przez piaskowanie, całość oczyszczania trwała ok. 1 godziny. Dalsze prace postępowały według schematu w jakim został oczyszczony obiekt powyżej, czyli przetarcie watą stalową, nałożenie Taniny, ponowne przetarcie watą stalowa, nałożenie Paraloidu B 44 i wosku.
Obiekt przed konserwacją:

(fot. A. Tomaszewska)
Obiekt po konserwacji:

(fot. A. Tomaszewska)
Dla poniższych powyższych przypadków najlepszą metodą było piaskowanie, gdyż dawało maksimum efektu i minimum zniszczenia materiału zabytkowego. Nie jest to reklamowanie jednego sposobu oczyszczania, bo dla jednych obiektów piaskowanie jest zabójcze a dla innych najlepsza metodą. Kluczem tego artykułu jest propagowanie wyboru metody, która jest najlepsza w danym przypadku, a nie to która z metod jest w ogóle najlepsza, gdyż takich nie ma. Każda z metod ma swoje wady i zalety i tylko wybór najwłaściwszej metody daje nam gwarancję jak najlepszego zabezpieczenia obiektu.
Istnieje bardzo wiele metod konserwacji, ale najważniejszą zasadą jest jej dobór w zależności od rodzaju obiektu. Daje to gwarancję że obiekt nie zatraci swoich wartości i przetrwa długi okres czasu a o to właśnie chodzi!!! Dbajmy o nasze przedmioty bo tworzą one historię o nas i naszych przodkach.
T.L.(Taz)
